在近期维适平®(精氨酸艾曲莫德片,VELSIPITY®)获 NMPA 批准的背景下,本文聚焦三个问题:
- 溃疡性结肠炎(ulcerative colitis, UC)的疾病负担正在发生什么变化?从流行病学趋势到发病机制,我们对这种疾病了解了多少?
- UC 的典型临床表现和自然病程有哪些特征?为什么它被称为”终身性疾病”?
- 在 Treat-to-Target 成为共识的背景下,UC 的诊断分层与阶梯治疗应如何理解?
2026 年 2 月 6 日,中国国家药品监督管理局(NMPA)批准精氨酸艾曲莫德片(商品名:维适平®,英文名:VELSIPITY®)的新药上市许可申请(NDA),由云顶新耀引进并在中国商业化,用于治疗对传统治疗或生物制剂应答不充分、失应答或不耐受的中度至重度活动性溃疡性结肠炎(ulcerative colitis, UC)成人患者[1]。
维适平®的获批,是近年创新药物加速进入 UC 领域的一个缩影。从监管视角看,无论是 FDA 的加速审批通道,还是 NMPA 近年来对严重疾病创新药实施的附条件批准和优先审评,均显著缩短了 UC 等免疫疾病新药从临床试验到上市的周期,也在客观上推动了更多基于替代终点和多区域临床试验(MRCT)的 UC 新药临床开发项目密集落地中国[2, 3]。
一、UC 药物市场与疾病负担:为什么值得关注?
这一趋势的背后,是持续扩容的全球 UC 药物市场——据 IMARC Group 预计,2024 年市场规模已达约 80 亿美元,未来十年仍将保持温和增长(预估复合年增长率为 4.82%)[4]。
对药企而言,这意味着 UC 不再只是”相对小众的免疫疾病”,而是一个已超过 80 亿美元、并将持续以约 5% 速度增长的成熟细分市场。
与此相应,全球 UC 药物管线也在持续扩容——仅在 7 大市场范围内,已有数十个针对 UC 的新分子实体处于 II/III 期临床开发阶段,涵盖 JAK 抑制剂、S1P 受体调节剂、IL 23 通路、微生物组治疗等多个靶点,UC 新药研发的密度和临床试验竞争程度都在快速上升[5]。在市场规模与管线密度的双重驱动下,UC 已成为全球炎症性肠病(inflammatory bowel disease,IBD)临床开发与 BD 及并购布局最活跃的治疗领域之一。
推动这一趋势的核心因素有三:UC 患者人数持续增加、疾病长期复发迁延带来的累积负担(每一次复发都意味着新一轮的治疗投入和生活质量损耗),以及高级治疗渗透率的逐步提升。三者共同重塑着 UC 的”疾病负担”(即患者数量、医疗支出与生活质量影响的综合体现)与”诊疗格局”。
在这样的背景下,本文从 UC 的基础事实出发——梳理疾病概述、流行病学现状、典型临床表现,以及现代诊断与风险分层框架,为理解当前 UC 领域的临床需求与治疗演进提供基础框架。
二、疾病概述与流行病学
溃疡性结肠炎(ulcerative colitis,UC)是炎症性肠病(inflammatory bowel disease,IBD)的一个亚型,特征是从直肠向近端连续累及结肠黏膜的慢性非特异性炎症,可反复发作、迁延不愈,是典型的终身性免疫介导疾病[6]。其发病率和患病率在全球范围内呈上升趋势[7]。
根据2025年美国胃肠病协会(AGA)临床指南更新引用的数据,炎症性肠病(IBD,包括溃疡性结肠炎和克罗恩病)的全球患病人数估计已超过800万[7]。作为 IBD 的主要亚型,UC 患者构成了这一巨大疾病负担的重要部分。在北美等高发病率地区,UC 的患病率已超过每 10 万人 400 例,意味着约 0.4% 的人口受累[6]。同时,在亚洲、拉丁美洲等既往的低发病率地区,UC 的发病率和患病率正在迅速上升[6, 9, 10]。发病高峰多在青壮年(20–40 岁),但儿童和老年人发病也在增加,儿童青少年 UC 的发病率在全球多地区呈持续上升趋势[6]。
中国过去被视为低发区,但最新 2023 版中国 UC 诊治指南特别强调,UC 正在成为我国重要的慢性消化病负担[11]。这种”患者越来越多、病程终身性、并发症与癌变风险并存”的特点,也正在驱动临床实践和卫生资源配置的持续调整。
三、发病机制与病理生理
UC 的确切病因尚不清楚,但主流共识认为:遗传易感个体在特定环境暴露下,肠道屏障、微生物群和黏膜免疫失衡共同作用,最终导致疾病发生[6]。
- 遗传因素:与克罗恩病(CD)相比,UC 的单个高危基因效应略弱,但多基因风险、多基因-环境交互更为重要[17]。
- 黏膜屏障受损:上皮紧密连接和黏液层受损,使细菌产物更易进入黏膜下层,触发免疫反应[18]。
- 肠道菌群失调:多项研究显示,UC 患者肠道微生物多样性下降、保护性菌群减少、致炎菌增多,微生物组成为重要创新治疗靶点[12]。
- 免疫失衡:涉及多种炎症通路,包括肿瘤坏死因子-α(TNF-α)、白细胞介素-12/23(IL-12/23)、Janus 激酶-信号转导和转录激活因子(JAK-STAT)、鞘氨醇-1-磷酸(S1P)等关键信号通路的异常激活[6, 13]。
病理上,UC 典型表现为直肠起始的连续性黏膜炎。重者可见黏膜糜烂、溃疡、脓性渗出;慢性期可见黏膜萎缩、假息肉。累及范围与严重程度直接对应临床分型和治疗策略。
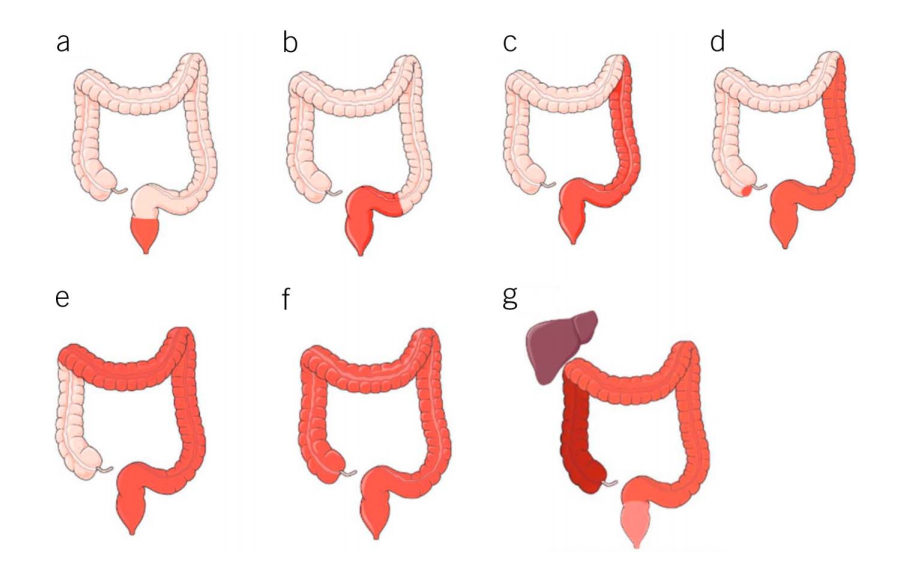
图1. 溃疡性结肠炎的不同临床表型。根据黏膜受累范围,传统上可将疾病分为孤立性直肠炎(a)、直肠乙状结肠炎(b)、左侧结肠炎(c)、广泛性结肠炎(d)和全结肠炎(e)(过去通过钡餐造影或内镜检查判断,近年则依靠组织学检查结果确定)。原发性硬化性胆管炎表现为相对或完全的直肠不受累(f),虽属于传统分类中的特殊类型,但其治疗方案与其它类型相似。阑尾周围或盲肠区域的病变(g)常见于远端结肠炎患者,其处理方式也与之相同[7]。
四、临床表现与自然病程
典型 UC 表现包括[6]:
- 肠道症状:反复发作的黏液脓血便、腹泻(轻者每日 3–4 次,重者可 >10 次)、里急后重、腹痛。
- 全身症状:乏力、体重下降、食欲差。重度或急性重症可出现发热、心动过速、贫血、低白蛋白血症。
- 肠外表现:关节炎或关节痛、结节性红斑、坏疽性脓皮病、葡萄膜炎、原发性硬化性胆管炎(PSC)等。
自然病程多为”发作–缓解–再发作”。急性重症溃疡性结肠炎(acute severe ulcerative colitis,ASUC)是 UC 的一种危重状态,据估计约 25% 的 UC 患者在其病程中至少会经历一次 ASUC 发作[12]。每次发作都伴随结肠切除术和死亡风险,需要紧急处理。
此外,由于长期慢性炎症反复损伤肠道黏膜,UC 患者的结直肠癌(colorectal cancer, CRC)风险较一般人群升高。不过,随着达标治疗推动黏膜愈合率提升、以及结肠镜监测的规范化普及,近年来 UC 相关 CRC 的年发病率已呈明显下降趋势[11]。
五、诊断:从”排除其他疾病”到”活动度与风险分层”
随着 UC 疾病负担逐步加重,诊疗理念也从过去的”能排除其他疾病即可”转向”通过精准分层支撑达标治疗”。诊断环节正在从单纯确诊,升级为贯穿全程管理的起点。
1)诊断流程:从排除性诊断到规范化确诊
国际与中国指南基本一致:诊断 UC 需要综合临床表现、内镜检查、组织病理学和实验室检查等多维度信息,并系统排除感染性结肠炎等其他可能病因[6, 7, 11]。
- 病史与体检:重点询问是否存在持续或反复血便、腹泻、里急后重等典型症状,同时了解用药史(NSAIDs、抗生素)、感染接触史及家族史。
- 实验室与粪便检查:常规检测包括血常规、CRP 或 ESR、肝肾功能及电解质。2025 年 ACG 指南强烈推荐对疑似 UC 患者进行粪便检测以排除艰难梭菌(C. difficile)感染,同时反对使用血清学抗体检测来建立或排除 UC 诊断或判断预后[7]。
- 内镜与活检:结肠镜检查是确诊 UC 的关键,应尝试进入回肠末端,并对受累及未受累区域均进行活检。病变范围应按蒙特利尔(Montreal)分类明确:直肠炎(E1)、左半结肠炎(E2)、广泛结肠炎(E3)[7, 11]。
- 影像:当怀疑存在穿孔、重度扩张等并发症,或需与克罗恩病进行鉴别时,CT、MR 或肠道超声可提供辅助信息。
2)评估疾病范围与活动度:为风险分层和达标治疗提供基线
确诊 UC 后,需进一步评估疾病范围与活动度。2025 年 ACG 指南主要从以下两个维度进行分型与评估[7]:
- 病变范围(Montreal 分类):
- E1(直肠炎,proctitis):炎症范围通常 ≤15 cm
- E2(左侧结肠炎):炎症超过直肠炎范围,但止于脾曲或脾曲以远
- E3(广泛性结肠炎):炎症延伸至脾曲以远;若整个直肠、结肠及盲肠均受累,则称为全结肠炎(pancolitis)
- 值得注意的是,即使内镜下看起来正常的近端结肠也可能存在组织学病变,因此应对内镜下未见炎症的近端区域单独取活检,以准确确定疾病范围及后续监测间隔。同理,即使直肠内镜下表现正常,也应单独取活检。
- 活动度:确诊后需立即并持续评估疾病活动度,以指导治疗决策和后续监测:
- 临床活动度:常用改良 Mayo 评分(亦称部分 Mayo 评分,含排便频率、便血、医师总体评价)或简单临床结肠炎活动指数(SCCAI)评估症状。Truelove & Witts 标准是定义急性重症 UC(ASUC)的经典依据。
- 内镜严重程度:必须采用经过验证的量表进行客观评估。Mayo 内镜评分(MES)是临床实践中最常用的工具,而UC 内镜严重程度指数(UCEIS)因定义更精确,更常用于临床研究及预后预测。
- 综合分层:基于临床、内镜及炎症标志物(如 C 反应蛋白、粪便钙卫蛋白),UC 活动度通常分为:缓解期、轻度活动、中度至重度活动、急性重症。其中”中度至重度”常被作为一个整体治疗决策区间。
- 关键点:治疗选择不仅取决于当前活动度,更应结合预后因素(如发病年龄 <40 岁、广泛性结肠炎、内镜下深溃疡、CRP 显著升高、低白蛋白血症)。存在 ≥2 个高危因素的患者,即使临床表现为轻度,也应按照中重度活动度的方案进行积极治疗。
表1. 改良 Truelove 和 Witts 疾病严重程度分型
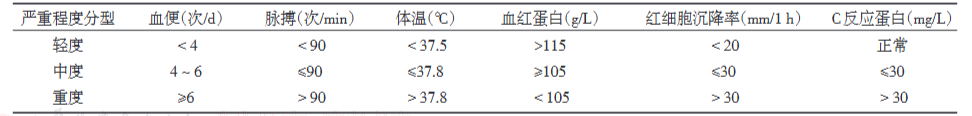
表2. 评估溃疡性结肠炎活动性的改良 Mayo 评分系统

注:a 每位受试者作为自身对照,从而评价排便次数的异常程度;b 每日出血评分代表一天中最严重的出血情况;c 医师总体评价包括 3 项标准,受试者对于腹部不适的回顾、总体幸福感和其他表现,如体格检查发现和受试者表现状态;总评分≤2 分且无单个分项评分>1 分为临床缓解,3 ~ 5 分为轻度活动,6 ~ 10 分为中度活动,11 ~ 12 分为重度活动;有效定义为评分相对于基线值的降幅≥30% 以及评分降幅≥3 分,而且便血的分项评分降幅≥1 分或该分项评分为 0 或 1 分。
表3. 溃疡性结肠炎 Mayo 内镜评分

表4. 溃疡性结肠炎内镜下严重程度指数(UCEIS)评分系统
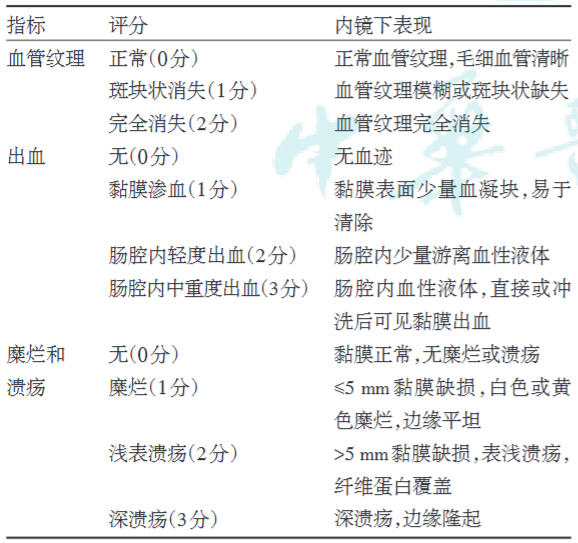
注:总评分为 3 个指标评分之和,正常:0 分,轻度活动:1 ~ 3 分,中度活动:4 ~ 6 分,重度活动:7 ~ 8 分
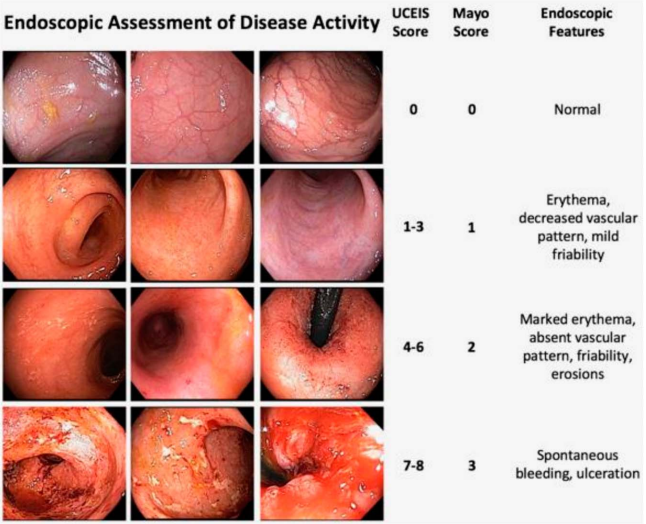
图2. 使用Mayo内镜评分系统和溃疡性结肠炎内镜严重程度指数(UCEIS)对溃疡性结肠炎患者进行的内镜图像样本[7]
2025 年 ACG 指南与中国 2023 版指南均强调”达标治疗(treat-to-target)”理念[7, 11, 14]:治疗目标应追求内镜改善(定义为炎症消退,Mayo 内镜评分为 0 或 1 分),以增加持续无激素缓解的可能性,并预防住院和手术。疾病评估和监测应结合患者报告结局、内镜评估以及粪便钙卫蛋白(FC)、C 反应蛋白(CRP)等炎症标志物。
六、治疗策略演进:基于严重程度的阶梯选择
现代 UC 治疗策略高度依赖疾病活动度的精确分层。
UC 的药物治疗分为两个阶段:
- 诱导缓解(induction of remission):即通过短期强化治疗控制活动性炎症、使疾病进入缓解状态;
- 维持缓解(maintenance of remission):即在达到缓解后持续用药以防止复发。治疗方案的选择取决于疾病活动度和病变范围。
1)轻中度活动性 UC
轻中度活动性 UC 的治疗核心是以 5-ASA 为基础的诱导与维持策略,治疗方案根据病变范围(E1/E2/E3)进行分层。据 2025 年 ACG 指南[7]:
- 诱导缓解:
- 直肠炎(E1):首选直肠用 5-氨基水杨酸(5-ASA)至少 1 g/日;若无效,可考虑他克莫司栓剂或倍氯米松栓剂。
- 左半结肠炎(E2):推荐直肠 5-ASA(至少 1 g/日)联合口服 5-ASA(至少 2.0 g/日),联合用药优于单用口服。
- 广泛结肠炎(E3):推荐口服 5-ASA 至少 2.0 g/日。
- 若口服与直肠 5-ASA 联合使用仍无效或不耐受,推荐加用口服布地奈德 MMX 9 mg/日诱导缓解;若 5-ASA 治疗整体失败,可考虑口服全身性糖皮质激素。
- 维持缓解:直肠炎推荐直肠 5-ASA(1 g/日);左半结肠炎或广泛结肠炎推荐口服 5-ASA(至少 1.5 g/日)。指南反对使用全身性糖皮质激素、布地奈德 MMX 或局部糖皮质激素进行维持治疗。
2)中重度活动性 UC
治疗目标是快速诱导临床与内镜缓解,并转向有效的维持治疗,避免长期使用激素。
据 2025 年 ACG 指南[7],诱导缓解有多种强推荐选择:
- 诱导缓解:
- 对于中度活动性 UC,可使用口服布地奈德 MMX 诱导缓解(强推荐)
- 口服全身性糖皮质激素
- S1P 受体调节剂(奥扎莫德、艾曲莫德)
- IL-12/23p40 抗体(乌司奴单抗)
- IL-23p19 抑制剂(古塞奇尤单抗、米利奇珠单抗、瑞莎奇珠单抗)
- 抗整合素药物(维多利珠单抗)
- 抗 TNF 药物(英夫利昔单抗、阿达木单抗、戈利木单抗)
- JAK 抑制剂(托法替布、乌帕替尼)
指南同时反对硫嘌呤或甲氨蝶呤单药用于诱导缓解。当使用英夫利昔单抗诱导时,推荐联合硫嘌呤以提高疗效。
- 维持缓解:原则上,使用哪种药物成功诱导缓解,就应继续使用该药物进行维持治疗。指南强烈反对使用全身性糖皮质激素维持缓解。
3)急性重症 UC(ASUC)
属于内科急症,需住院治疗。
据 2025 年 ACG 指南[7],ASUC 的管理流程如下:
- 入院评估:强推荐对 ASUC 患者进行艰难梭菌(CDI)检测,并应评估有无中毒性巨结肠。所有患者应在入院后 72 小时内(最好 24 小时内)完成软式乙状结肠镜检查,评估炎症严重程度并排查巨细胞病毒(CMV)结肠炎。
- 一般管理:强推荐药物性深静脉血栓(DVT)预防,同时反对常规使用广谱抗生素。
- 初始治疗:推荐静脉用糖皮质激素——甲基强的松龙 60 mg/日或氢化可的松 100 mg 每日 3–4 次。
- 挽救治疗:若静脉糖皮质激素治疗 3 天后反应不佳,推荐英夫利昔单抗或环孢素作为挽救治疗药物。
值得注意的是,随着上述新机制药物竞相进入临床,UC 相关的注册性临床试验数量在过去 10–15 年内呈持续上升趋势,且从单臂、单一终点逐步演进为随机、双盲、多终点设计,对内镜缓解、组织学缓解等”硬终点”的依赖显著增加[15],这也客观抬高了 UC 临床开发对专业 CRO 的需求门槛。
七、写在最后
伴随全球及中国 UC 患者数量持续上升、发病年龄前移以及长期复发迁延,溃疡性结肠炎已经从教科书里的”消化科小专病”,逐渐演变为需要全程管理和多学科协作的慢病负担。
从本文梳理的疾病概述、流行病学、临床表现以及”从排除诊断走向分层管理”的诊断框架可以看到,UC 的临床实践正朝着更早识别高危人群、更精细化评估疾病活动度和风险的方向演进。2025 年 ACG 指南的更新,进一步强化了以内镜愈合为核心的治疗目标,并为轻、中、重度及急性重症 UC 提供了详尽的、基于 GRADE 分级的循证治疗路径。
在这样的基础之上,靶向生物制剂、口服小分子等创新疗法才有机会通过合理的序贯与组合策略真正改善结局。然而,系统综述仍反复强调:在真实世界中,能长期达到”无激素缓解+黏膜愈合”的 UC 患者仍是少数,疗效”天花板”、长期安全性和序贯/联合策略仍存在显著未满足的临床需求(unmet clinical needs)[15, 16],这也是全球 UC 新药临床开发和适应症扩展的核心驱动力。
本文梳理了 UC 的疾病基础与诊疗现状,为理解该领域的临床需求与研发方向提供了框架。随着更多创新疗法进入临床,UC 的治疗格局仍值得持续关注。
参考文献
[1] 云顶新耀. 云顶新耀维适平®获中国国家药品监督管理局批准上市 为中重度溃疡性结肠炎治疗提供新选择 [EB/OL]. (2026-02-06) [2026-02-24].
[2] Zheng L, Wang W, Sun Q. Targeted drug approvals in 2023: breakthroughs by the FDA and NMPA. Signal Transduct Target Ther. 2024;9:46.(用于支持 FDA/NMPA 加速审批在免疫疾病领域的常态化趋势)
[3] Sun J, et al. Confirmatory Trials for Drugs Granted Conditional Approval by the Chinese National Medical Products Administration. JAMA Health Forum. 2024;5(12):e244469.(用于支持 NMPA 附条件批准政策及其对创新药上市周期的影响)
[4] IMARC Group. Ulcerative Colitis Market: Global Industry Trends, Share, Size, Growth, Opportunity and Forecast 2025-2033. [EB/OL]. [2026-02-24]. https://www.imarcgroup.com/ulcerative-colitis-market[1] (用于支持全球 UC 药物市场规模与增长率预测)
[5] Zurba Y, Gros B, Shehab M. Exploring the Pipeline of Novel Therapies for Inflammatory Bowel Disease; State of the Art Review. Biomedicines. 2023;11(3):747.(用于支持全球 UC 在研管线数量、靶点多样性及 II/III 期临床开发密度)
[6] Gros B, Kaplan GG. Ulcerative Colitis in Adults: A Review. JAMA. 2023;330(10):951-965.(用于支持北美患病率、发病率变化趋势、发病机制靶点及治疗药物分类)
[7] Rubin DT, Ananthakrishnan AN, Siegel CA, et al. ACG Clinical Guideline Update: Ulcerative Colitis in Adults. Am J Gastroenterol. 2025;120:1187-1224.(2025 年美国胃肠病学会(ACG)最新临床指南,提供诊断、治疗、监测的全面循证推荐)
[8] Singh S, Ananthakrishnan AN, Nguyen NH, et al. AGA Clinical Practice Guideline on the Role of Biomarkers for the Management of Ulcerative Colitis. Gastroenterology. 2023;164(3):344-372.(用于说明全球 IBD 疾病负担及生物标志物 FC 的作用)
[9] Ng SC, et al. Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies. Lancet. 2017;390(10114):2769-2778.(用于支持全球发病率、患病率变化趋势,特别是新兴工业化国家的增长)
[10] Buie MJ, et al. Global Hospitalization Trends for Crohn’s Disease and Ulcerative Colitis in the 21st Century: A Systematic Review with Temporal Analyses. Clin Gastroenterol Hepatol. 2023;21(9):2212-2223.e15.(用于支持不同流行病学阶段地区的住院率变化趋势)
[11] 中华医学会消化病学分会炎症性肠病学组. 中国溃疡性结肠炎诊治指南(2023 年·西安)[J]. 中华炎性肠病杂志(中英文), 2024, 8(1):1-50.(用于支持中国指南诊断标准、评估方法及治疗目标)
[12] Rivière P, et al. Acute severe ulcerative colitis management: unanswered questions and latest insights. Lancet Gastroenterol Hepatol. 2024;9(3):251-262.(用于支持 ASUC 的发生率、风险及定义)
[13] Raine T, Bonovas S, Burisch J, et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment. J Crohns Colitis. 2022;16(1):2-17.(用于支持治疗原则、药物推荐等级及 ASUC 管理)
[14] Peyrin-Biroulet L, et al. Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE): Determining Therapeutic Goals for Treat-to-Target. Am J Gastroenterol. 2015;110(9):1324-1338.(用于支持”达标治疗”的核心理念与目标)
[15] Fanizzi F, Allocca M, Fiorino G, et al. Raising the bar in ulcerative colitis management. Therap Adv Gastroenterol. 2024;17:17562848241273066.(用于支持 UC 临床试验终点从症状向内镜/组织学升级的趋势,以及深度缓解率仍有限的 unmet need)
[16] Irving PM, Hur P, Gautam R, Guo X, Vermeire S. Real-world effectiveness and safety of advanced therapies for the treatment of moderate-to-severe ulcerative colitis: Evidence from a systematic literature review. J Manag Care Spec Pharm. 2024;30(9):1026-1040.(用于支持高级治疗在真实世界中的疗效局限与数据空白)
[17] Caron B, Honap S, Peyrin-Biroulet L. Epidemiology of Inflammatory Bowel Disease across the Ages in the Era of Advanced Therapies. J Crohns Colitis. 2024;18(Supplement_2):ii3-ii15.(用于支持 IBD 遗传易感性中多基因风险与基因-环境交互的重要性)
[18] Muzammil MA, Fariha F, Patel T, et al. Advancements in Inflammatory Bowel Disease: A Narrative Review of Diagnostics, Management, Epidemiology, Prevalence, Patient Outcomes, Quality of Life, and Clinical Presentation. Cureus. 2023;15(6):e41120.(用于支持 UC 黏膜屏障受损机制——上皮紧密连接与黏液层损伤的病理生理基础)
撰稿人:周安楠
审核:陈亚红
排版:周安楠



