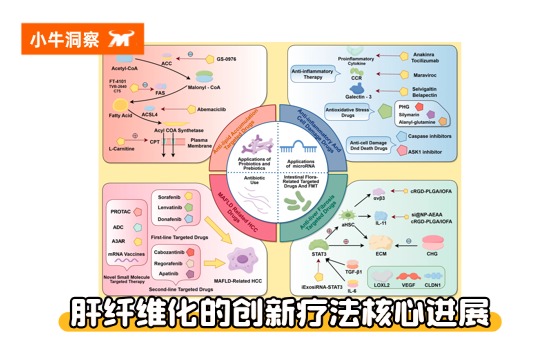
前言
创新药物的研发与临床研究中常常会面临一个问题:即针对特殊人群的临床用药该如何把握剂量与使用频次。上图为截取FDA批准的某一新药的药品说明书部分目录内容,其中第8条对于特殊人群:妊娠/哺乳期女性、儿童用药、老年人用药以及肝/肾损伤患者的用药均有描述,因特殊人群的机体组成和生理功能有普通人群有许多的区别,这些特点能影响药物在体内的吸收、分布、代谢和排泄过程,因此需要格外关注此类人群的用药方案。
为什么需要进行肝功能损害患者的药代动力学研究?

在过去的几十年,肝脏疾病成为全球导致死亡和疾病的主要原因之一。根据Global Burden of Disease project,在2010年,有200多万人死于包括急性肝炎、肝硬化和肝癌等重大肝病,约占全球所有死亡人数的4%。据估计,中国超过五分之一的人口受到肝脏疾病的影响,包括乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)感染、肝硬化、肝癌、非酒精性脂肪性肝病(NAFLD)、酒精相关肝病(ALD)和药物性肝损伤(DILI)等。
参考2012年CDE颁布《肝功能损害患者的药代动力学研究技术指导原则》,通过多种氧化和结合代谢途径,以及药物原型或代谢产物通过胆汁排泄,肝脏参与许多药物的清除。肝功能损害引起的药物排泄和代谢活动的改变,可能导致药物蓄积,或在少数情况下无法形成活性代谢物。肝脏作为人体内药物代谢的主要器官,表达多种代谢酶与转运体。大量文献证实,肝脏疾病可以改变药物吸收和分布过程,进而改变药物的安全性和有效性。即便在肝脏并非主要负责某药物清除的器官时,肝脏疾病同样可能会改变肾脏功能,并且该影响是不确定的,尤其是对药物的药代动力学(PK)和药效动力学(PD)的影响。
总的来说,临床上尚没有有效地预测药物PK和PD的肝功能指标。但是,在药物开发期间,在肝功能受损患者中进行的临床研究可提供相关信息,有助于确定这些患者的临床用药起始方案。
哪些情况下需要进行肝功能损害患者的药代动力学研究?
1、需要进行肝脏损害患者的PK研究:
1)如果肝脏代谢和/或排泄的量占原型药物或活性代谢产物清除量的相当大部分(大于所吸收药物的20%),推荐在肝功能损害患者中进行 PK 研究。
2)如果药品说明书或文献资料提示该药为一种治疗范围窄的药物时,即便该药物和/或活性代谢产物经肝脏消除的量较少(<20%),也建议进行肝脏损害患者的 PK 研究。
2、一般不需要进行肝脏损害患者的PK研究:
1)药物完全通过肾脏清除途径排泄,不涉及到肝脏。
2)小部分药物(<20%)在肝脏代谢,并且药物治疗范围宽,因此,肝脏清除能力的轻度损害不会直接或通过增加与其他药物的相互作用而产生药物毒性。
3)药物为气态或挥发性的,并且药物及其活性代谢产物主要通过肺部清除。
4)对于仅单剂量使用的药物,一般不需要进行肝脏损害患者的药代动力学研究。
肝功能损害患者PK研究的临床试验设计
1、受试者的选择
肝功能正常对照组的受试者应来自于目标治疗患者,而非健康志愿者。2003年,FDA颁布指导原则《Pharmacokinetics in Patients with Impaired Hepatic Function: Study Design, Data Analysis, and Impact on Dosing and Labeling》,提出为了在整个肝损伤范围内制定特定的剂量建议,应该在三类Child-Pugh分级:轻度、中度和重度以及对照组的患者中进行研究(如表1所示)。
应用该分级方法,将根据两种临床特征(脑病和腹水)和三种实验室指标(血清白蛋白、血清胆红素和凝血酶原时间)对受试者进行分组。将肝脏机能障碍分为A、B和C组,或对应于5~6 分,7~9分和10~15分,分别是“轻度”、“中度”和“重度”。
表1 Child- Pugh分级标准

Case:某医院肝损患者Child Pugh分级

但Child-Pugh分级标准也具有一定局限性,例如:Child-Pugh 分级评分主要作为肝硬化患者的分级标准制定的,对于非肝硬化患者使用本分级标准是否恰当有待商榷;白蛋白、胆红素等指标可能受其他与肝功能障碍无关的因素的影响,如炎症、营养状况等;Child-Pugh 分级评分仅能将患者分为 A、B、C 级,取值也仅5~15 分,评分缺乏连续性且具有明显的穹顶效应,且难以对腹水与肝性脑病作出客观准确的分级,主观性强、敏感性较差等。
美国国家癌症研究所(NCI)同样有关于肝功生化指标的分级标准(如表2所示),该分级标准仅关注总胆红素和门冬氨酸氨基转移酶两个关键指标,其优点是胆红素、AST为评价肝功能关键指标,临床操作容易简单方便,且生化指标不受主观因素影响,分级更加明确简单,然而,仅考虑单一肝功生化指标,存在一定局限性,未能全面考察肝损病人各项指标状态,并且临床试验中,此分级标准对于中重度肝损病人的招募产生一定难度。
表2 美国国家癌症研究所(NCI)肝功生化指标分级标准
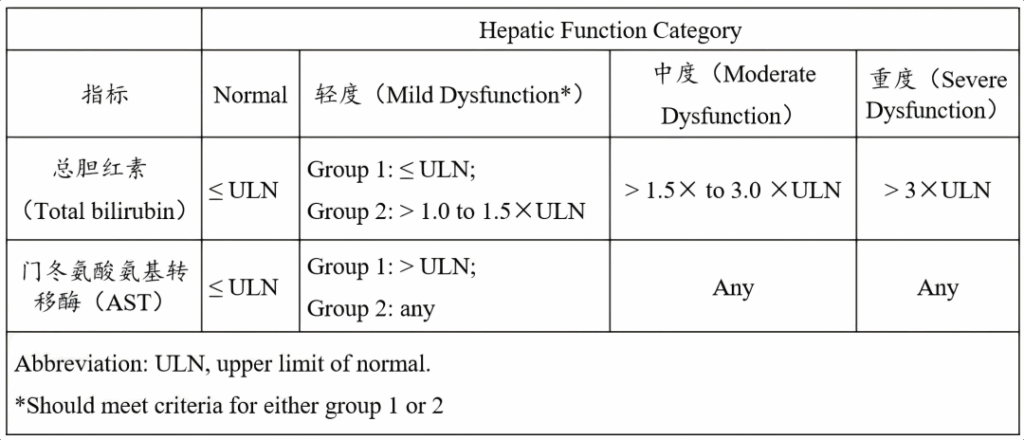
2、试验分组
研究分可为三个组别,入组24例受试者,其中A组:轻度肝功能不全受试者(Child-Pugh A级)8例、B 组:中度肝功能不全受试者(Child-Pugh B级)8例、C组:肝功能正常受试者8例(C组人群的选择应与肝损害病人在年龄、性别、体重、遗传多态性和其它可潜在显著影响药代动力学的因素方面具有可比性)。
当中度肝功能不全受试者安全性可耐受、PK参数与肝功能正常受试者相比无显著差异时,如有必要,可能继续入组4-8例重度肝功能不全的受试者(D组,Child-Pugh C级)进行研究。
3、样本采集和分析
由于肝功能损害的受试者肝脏代谢能力下降,因此需要恰当地设定样品采集时间,确定药物及其活性代谢产物的半衰期,采集足够的时间血样,使其包含:吸收、分布、消除相。其中吸收相部分取2-3个点;峰浓度附近至少3个点;末端消除相取3-5个点。对于那些可以被肝脏大量摄取(摄取率>0.7)和高血浆蛋白结合率(未结合部分<10%)的药物,建议至少在血浆浓度的谷值和峰值处测定游离药物比率。
4、界值设定
根据CDE于2012年颁布《肝功能损害患者的药代动力学研究技术指导原则》,一般需考虑如下两方面:
1)如果肝损害对药物PK的影响非常明显(如,AUC增加两倍或更多),应在产品说明书中推荐进行剂量调整。并进一步考虑加做重度肝功能不全患者及与之匹配的健康人的药物代谢动力学研究。
2)如果肝损害对药物PK的影响较小,即所得主要药动学参数AUC和Cmax90%置信区间落入标准的80%~125%范围,且未发现不等效的其他信息,可以得出肝损害对药物PK无影响(指无临床意义的影响)的结论。