AGA是临床最常见的脱发类型。我国脱发人群大约在2亿左右,平均每6个人中就有一位受脱发困扰,并且脱发人群的数量每年正在以至少15%的速度不断增加。
在对抗雄激素性脱发(AGA)的漫长征程中,我们是否已经触及天花板?米诺地尔与非那雄胺(两者都已有口服、外用等多种剂型产品上市)之后,路在何方?
何首乌(Polygoni Multiflori Radix)在中医中长期用于治疗脱发和白发。现代研究已发现其含有二苯乙烯类、蒽醌类等活性成分,但其完整的作用机制,特别是植物外泌体的作用尚未被充分探索。植物外泌体样纳米颗粒(PENs)作为天然纳米载体,可能通过携带植物miRNA实现跨界基因调控,但其在人类生理中的作用未被充分探索。
近日北京大学团队发布在《Pharmacological Research》期刊上的一项重磅研究结果表明传统生发中药何首乌中的植物外泌体样纳米颗粒(PMENs)能够作为天然载体,实现跨物种基因调控,或许能为治疗AGA开辟一条全新的路径。
一、认知革命:从“传统中药”到“基因信使”
以往针对何首乌的研究,重点聚焦在二苯乙烯苷、蒽醌类等小分子成分及其功效上。北大团队独辟蹊径,将核心放在了其自身分泌的纳米级外泌体(PMENs)上,成功从其根部提取出粒径约77纳米的PMENs。这一发现将何首乌的研究从”化学成分”纬度拓展至”生物信息纳米载体”纬度,其奥秘或许不仅仅在于其“化学成分”,他派出的天然 “纳米信使小队” 亦举足轻重。
二、精准制导:直击AGA的“指挥中心”
这支“小队”如何工作?我们一起来看看他的精准的作战路线(见图1):
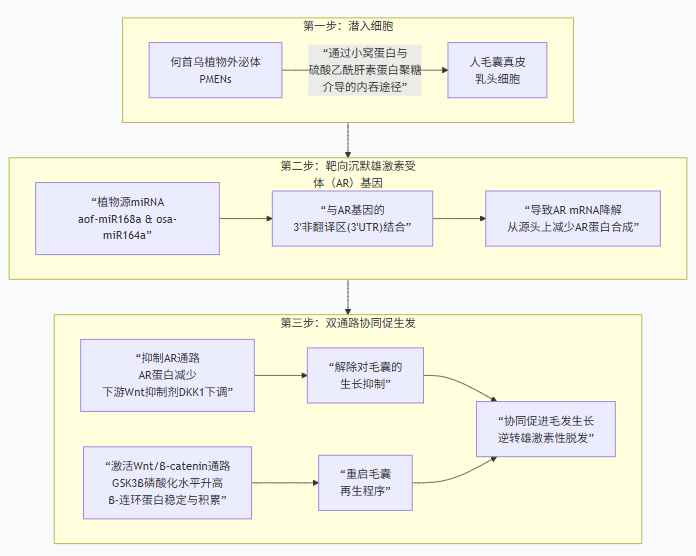
图1
- 潜入细胞: PMENs通过小窝蛋白和硫酸乙酰肝素蛋白聚糖(HSPG)介导的内吞途径进入细胞。实验表明,使用特定抑制剂阻断该途径后,PMENs的细胞摄取率可被抑制高达86.85%,展现了其高效的组织靶向性。由此可高效“潜入”人类毛囊真皮乳头细胞。
- 靶向沉默:这是机制的核心。高通量测序发现PMENs中富含的aof-miR168a和osa-miR164a与人类AR基因3’非翻译区存在高度互补性(如图2),预示强大的结合潜力。 aof-miR168a 和 osa-miR164a能像“精确制导导弹”一样,直接找到并结合导致AGA的核心祸首——雄激素受体(AR)基因的3’非翻译区(3’UTR)。这种结合导致AR的mRNA被降解,从源头上减少了“致病指挥官”(AR蛋白)的数量。实验证实,PMENs处理可使毛囊细胞中AR蛋白水平最高下降23.2%。
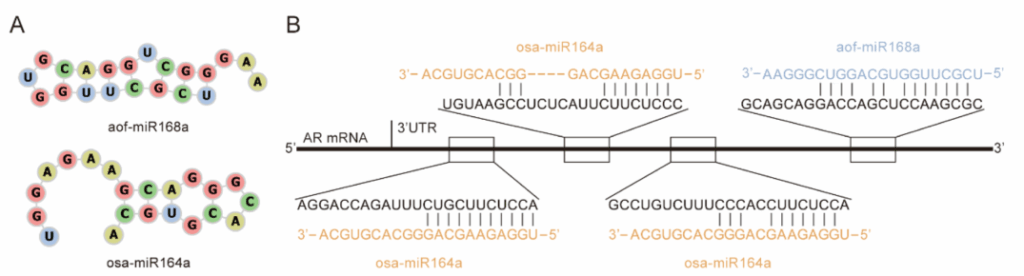
图2
这一机制使得疗法从传统的“干扰信号”升级为从基因层面“直接减少指挥官”,实现了对AGA更根本的干预。
三、双通路协同:不仅治标,更能生发
更令人振奋的是,PMENs的作用并非单一抑制。在抑制AR的同时,通过提升GSK3β磷酸化水平(最高31.0%),稳定β-连环蛋白(最高45.6%),从而强力激活了负责毛囊再生和生长的Wnt/β-catenin信号通路。
这就好比在击败敌人的同时,还为我方部队补充了强大的粮草和装备。这一双重机制,协同作用,不仅能阻止脱发阻止毛囊微型化,更能有效促进毛囊再生。
四、动物实验:效果优于米诺地尔
理论很完美,实践结果如何呢?
在睾酮诱导的脱发小鼠模型中,PMENs治疗组在毛发再生速度和最终密度上均优于米诺地尔组(值得一提的是,小编认为未来如果能增加非那雄胺(另一当下主流的治脱药物)作为对照组,将使研究结论更具说服力)。特别是在更具挑战性的脱发模型中表现更为出色,为其下一步临床研究提供了有力支持,为临床应用前景提供了有力证据。
五、未来展望:开启RNA纳米药物新时代
业界认为这项研究的价值远超一种新成分的发现。
它首次揭示了,传统中药的天然纳米颗粒,可以作为一种高效、安全的载体,进行跨物种的基因调控。这不仅为雄激素性脱发的治疗,更为整个RNA药物领域开辟了一条全新的技术路径。预示着未来可能很多情况下不再需要复杂的人工合成载体,大自然已为我们准备了精准的”纳米信使”。
参考文献:
- Li S, Zhang Y, Liu X, et al. Cross-kingdom delivery and putative gene modulation of androgen pathways by plant-derived exosome-like nanoparticles from polygoni multiflori radix promotes hair growth via miRNA cargo. Pharmacological Research, 2025, 222: 108033.
编辑:郑叶敏
校对排版:周安楠